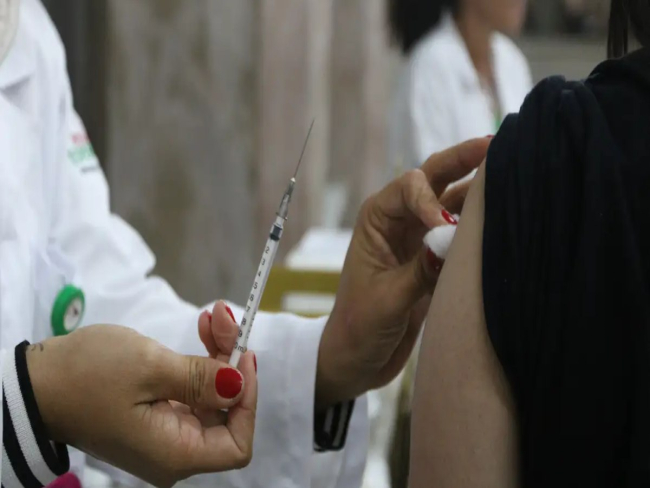
Rovena Rosa – Agência BrasilO estudo será realizado em sete cidades e busca gerar evidências para uma possível incorporação do medicamento ao Sistema Único de Saúde (SUS)
A Fundação Oswaldo Cruz (Fiocruz) iniciará testes de uma nova injeção semestral para prevenção ao HIV no Brasil. O estudo será realizado em sete cidades e busca gerar evidências para uma possível incorporação do medicamento ao Sistema Único de Saúde(SUS).
As cidades escolhidas para participar do teste foram Campinas (SP), Florianópolis, Manaus, Nova Iguaçu (RJ), Rio de Janeiro, Salvador e São Paulo.
Segundo a Anvisa, o medicamento da fabricante Gilead Sciences é indicado para adultos e adolescentes a partir de 12 anos, com peso mínimo de 35 kg, que estejam sob risco de contrair o vírus. Antes de iniciar o tratamento, é obrigatório realizar teste com resultado negativo para HIV-1.
O estudo leva o nome de ImPrEP LEN Brasil e será voltado a homens gays e bissexuais, pessoas não binárias identificadas como só sexo masculino ao nascer e pessoas transgênero, de 16 a 30 anos.
Sobre a injeção
O medicamento que será usado para os testes é o lenacapavir, uma forma de profilaxia pré-exposição (PrEP) ao HIV. Ele foi aprovado pela Anvisa em 12 de janeiro e pode ser usado em versão injetável, que será utilizada no estudo, ou em comprimidos. A droga age em diferentes etapas do ciclo de replicação do vírus, o que aumenta seu potencial preventivo. O fármaco tem alta eficácia contra o vírus e, como injeção subcutânea, precisa ser administrado a cada seis meses.
Quando começam os testes?
A Fiocruz confirmou que as doses já foram disponibilizadas pela Gilead Sciences, mas que o início das aplicações depende da chegada de agulhas específicas ao Brasil.
Expectativa sobre os custos e implementação no SUS
Apesar do progresso científico, o alto custo do medicamento ainda é visto como um obstáculo. De acordo com um estudo publicado na revista The Lancet, o custo real de fabricação poderia ficar entre US$ 25 e US$ 46 por pessoa ao ano. No entanto, nos Estados Unidos, o valor do tratamento anual pode ultrapassar US$ 28 mil por paciente (aproximadamente R$ 150,6 mil na cotação atual).
No Brasil, o preço do medicamento ainda não foi estabelecido. Conforme informou a Anvisa, o teto de valor deverá ser definido pela Câmara de Regulação do Mercado de Medicamentos (CMED).
Para que o remédio seja disponibilizado pelo SUS, será necessária uma avaliação técnica da Comissão Nacional de Incorporação de Tecnologias no SUS (Conitec), seguida de uma decisão final do Ministério da Saúde.
Em nota, a Gilead Sciences afirmou que o preço de comercialização no Brasil ainda não foi determinado e que comparações com valores de outros países não refletem o processo adotado no país. A empresa também destacou que não há previsão para uma eventual incorporação ao SUS, uma vez que os trâmites seguem prazos específicos.
Escolha das cidades para os testes
O critério de seleção dessas cidades não foi divulgado até o momento, mas alguns fatores como: impacto epidemiológico do HIV, diversidade regional, presença de serviços de saúde preparados para pesquisa, e capacidade de recrutar populações-chave para avaliar a viabilidade da nova estratégia de prevenção no Brasil, podem ter sido avaliados e ter tido influência na escolha de capitais e grandes metrópoles.
Fonte: SAUDE.IG.COM.BR